Ossigeno
L'ossigeno è il primo elemento del sesto gruppo del sistema periodico ed è caratterizzato dalla presenza di 6 elettroni nel suo livello più esterno. In natura è costituito da una miscela di tre isotopi: 16O, 17O, 18O di cui il primo, essendo presente nella misura del 99,8%, è l'isotopo predominante. La formula di struttura della sua molecola è la seguente:
![]()
Sulla crosta terrestre l'ossigeno, combinato principalmente sotto forma di ossidi, di carbonati e di silicati, è l'elemento più abbondante e ne costituisce circa il 50% in peso. Lossigeno si trova, inoltre, allo stato combinato nell'acqua, in numerosi acidi, nei sali ossigenati e nei composti organici.
L'ossigeno si presenta libero in natura in forma di molecole biatomiche gassose e relativamente molto solubili in acqua (in condizioni normali si sciolgono 32 ml/l di ossigeno in acqua). Esso è l'elemento principale della respirazione ed è, quindi, il maggior responsabile dello svilupparsi del calore animale. In circostanze d'emergenza l'ossigeno viene somministrato agli animali e all'uomo particolarmente puro e pressurizzato, per garantire cicli vitali in pericolo.
Nell'aria atmosferica è il secondo componente in ordine di abbondanza e, nonostante le grandi quantità consumate dalla respirazione degli organismi viventi, dalla putrefazione, dalle combustioni e dalla graduale ossidazione delle rocce della crosta terrestre, la sua concentrazione media rimane praticamente costante. Il suo consumo viene quasi completamente compensato dall'ossigeno che viene immesso nell'atmosfera dai processi metabolici delle piante. È ben noto, infatti, il suo ruolo nella respirazione delle piante e degli animali.
| Composizione media dell'aria secca | |
| Componenti | Volume % |
| azoto | 78,09 |
| ossigeno | 20,95 |
| argo | 0,92 |
| anidride carbonica | 0,035 |
| idrogeno | 0,01 |
| neon | 0,0016 |
| elio | 0,0005 |
| metano | 0,0002 |
| kripto | 0,0001 |
| xeno | 0,00006 |
Come si vede dalla tabella sopra riportata, lossigeno costituisce circa il 21% in volume dellaria, mentre allo stato combinato costituisce l89% in peso di tutta lacqua.
Nell'uomo l'ossigeno inspirato nei polmoni dall'atmosfera viene assorbito dall'emoglobina del sangue e inviato alle cellule che lo utilizzano per la respirazione dei tessuti.
Durante la respirazione i carboidrati vengono ossidati fornendo così l'energia richiesta per l'attività cellulare. Poiché l'ossigeno è un ossidante lento è necessario l'intervento di opportuni catalizzatori biologici (enzimi) per accelerare le reazioni ossidative che così possono avvenire alla temperatura corporea.
Proprietà dellossigeno
A temperatura ambiente l'ossigeno è un gas costituito da molecole biatomiche che soltanto in determinate condizioni (sotto l'azione di scariche elettriche) si trasforma, sia pure parzialmente, in ozono (O3), che è una sua forma allotropica instabile tendente a trasformarsi in ossigeno biatomico. Allo stato libero l'ossigeno è un gas incolore, inodore e scarsamente solubile in acqua ma, comunque, in misura sufficiente da consentire le attività respiratorie degli organismi acquatici. Le sue costanti chimico-fisiche sono riassunte nella tabella seguente:
| numero atomico | 8 |
| peso atomico | 15,999 |
| configurazione elettronica | 2s22p 4 |
| potenziale di ionizzazione | 13,61 eV |
| affinità elettronica | 1,48 eV |
| elettronegatività | 3,5 |
| punto di fusione | -218,8 °C |
| punto di ebollizione | 182 °C |
A temperatura ambiente lossigeno è poco reattivo e gli elementi che in tali condizioni si combinano con esso sono relativamente pochi. Tale combinazione viene accelerata dalla presenza di tracce di umidità. A temperatura elevata l'ossigeno diventa fortemente reattivo così che, ad esempio, una spira rovente di ferro in atmosfera di ossigeno puro brucia con fiamma abbagliante trasformandosi in Fe2O3. Nella maggior parte dei composti (ossidi, acidi, sali, ecc.) il suo stato di ossidazione è -2 mentre nei perossidi, come H2O2 e Na2O2, ha numero di ossidazione -1. Soltanto con il fluoro, che è l'unico elemento che lo supera in elettronegatività, ha numero di ossidazione +2 (fluoruro di ossigeno, OF2).
Preparazione dellossigeno
In laboratorio lo si ottiene in piccole quantità per azione del calore su ossidi o sali minerali ricchi di ossigeno come il clorato di potassio (KClO3) e l'ossido di mercurio (II) (HgO).
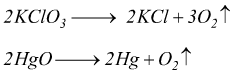
Industrialmente, l'ossigeno, veniva largamente preparato mediante l'elettrolisi dell'acqua (soluzioni al 20-30% di NaOH o KOH), ma tale metodo è stato del tutto soppiantato a causa degli elevati costi dell'energia elettrica e sostituito dalla distillazione frazionata dell'aria liquida che fornisce ossigeno puro con un titolo che supera il 95%. Nel disegno seguente è riportato lo schema di un impianto per la produzione di aria liquida dalla quale per distillazione si ottiene ossigeno biatomico puro.

Utilizzo dell'ossigeno
L'ossigeno è molto usato come comburente nei cannelli ossidrici e ossiacetilenici e negli apparecchi per la respirazione, sia per gli usi clinici che per i respiratori usati da sommozzatori, aviatori e astronauti. maggiori consumi (63% circa) si hanno comunque nelle acciaierie e nella siderurgia in generale, nei processi di conversione della ghisa in acciaio. Notevoli quantità di ossigeno vengono oggi assorbite nell'industria missilistica che lo utilizza come comburente per i motori dei razzi. L'ossigeno viene commercializzato in bombole di acciaio che usano il bianco come colore distintivo che, però, a causa della loro limitata capacità, sono sempre più spesso sostituite da serbatoi di grandi dimensioni, nei quali l'ossigeno è contenuto allo stato liquido. Sotto forma di ozono, grazie al suo elevato potere ossidante, è usato come agente sbiancante, disinfettante e nella potabilizzazione delle acque. Quest'ultimo uso, nonostante il costo più elevato, viene preferito alla clorazione che dà all'acqua cattivo sapore.
Combustione
Le combinazioni dell'ossigeno con i vari elementi si dicono ossidazioni
se sono lente e se avvengono praticamente a freddo, mentre si definiscono
combustioni se sono rapide e calorifiche.
La parola combustione, indica infatti un processo di ossidazione rapido
che avviene con emissione di luce e calore (fiamma) durante il quale l'energia
chimica si degrada in energia termica Così, il ferro si ossida mentre il
carbonio brucia combinandosi con l'ossigeno.
Generalmente quando si parla di combustioni ci si riferisce a processi di ossidazione rapida mediante ossigeno, ma sono combustioni anche ossidazioni rapide che hanno luogo in assenza di questo gas: ad es. l'idrogeno brucia in ambiente di cloro (con fiamma) formando acido cloridrico.
Una reazione di combustione aumenta la propria velocità all'aumentare della temperatura; per bassi valori di questa la combustione avviene lentamente, quindi, senza sensibile sviluppo di calore, che viene dissipato man mano che si produce.
Esiste una soglia di temperatura, chiamata temperatura di ignizione, oltre la quale si verifica la combustione vera e propria, con emissione di luce e di calore. Le combustioni lente possono trasformarsi spontaneamente in combustioni rapide se la quantità di calore da esse sviluppato non viene sufficientemente smaltito man mano che si produce.
Ozono
L'ossigeno può presentarsi in secondo una diversa configurazione atomica ( forma allotropica ) chiamata ozono; questo è un gas di odore caratteristico e di colore blu poco intenso. L'ozono è una specie molecolare instabile, altamente ossidante, perché decomponendosi sviluppa ossigeno atomico.
![]()
Per questo motivo l'ozono è usato come battericida in odontoiatria e nell'igiene delle acque. L'ozono si può preparare sottoponendo a scariche elettriche o irradiando con luce ultravioletta l'ossigeno:
![]()
Le radiazioni ultraviolette solari hanno provocato, attraverso milioni di anni, il formarsi di una statisticamente invariabile coltre d'ozono attorno alla Terra. Tale fascia gassosa protegge da quelle micidiali radiazioni i viventi terrestri: solo così è possibile la vita sulla Terra.
 edutecnica
edutecnica