Idrogeno
L'idrogeno è il primo elemento della tavola periodica avendo un solo protone nel nucleo e un solo elettrone nell'orbitale 1s. Non si trova libero in natura, tranne che nei gas vulcanici, ma è l'elemento più abbondante nell'universo essendo il principale costituente delle stelle e della materia interstellare; nel sole.
Si valuta che l'idrogeno costituisca il 97% in peso della materia cosmica e meno dell'1% in peso della materia terrestre.
L'idrogeno naturale è una miscela di tre isotopi costituita per il 99,9%
da protio (1H simbolo H),
per lo 0,016% da deuterio (2H
simbolo D) e da trizio
(3H simbolo T ), che è l'isotopo radioattivo
i cui nuclei si decompongono spontaneamente emettendo radiazioni β.
Combinato, invece, l'idrogeno è molto diffuso: costituisce lo 0,76% della
crosta terrestre e l'11,2% dell'acqua che è il suo principale composto;
entra a far parte degli idrocarburi ed è il componente fondamentale di tutti
i composti organici animali e vegetali e della materia vivente; basti ricordare
che nel corpo umano è presente nella misura del 10%.
L'idrogeno a temperatura ambiente è un gas incolore, inodore e insapore. Le sue costanti chimico-fisiche sono riassunte nella tabella seguente.
| numero atomico | 1 |
| peso atomico | 1.008 |
| peso molecolare | 2,016 |
| configurazione elettronica | 1s |
| potenziale di ionizzazione | 13,59 eV |
| affinità elettronica | 0,752 eV |
| elettronegatività | 2,1 |
| punto di fusione | -259,23 °C |
| punto di ebollizione | -252,77 °C |
| energia di legame | 30 kJ/mol |
| peso specifico | 0,0899 g/l |
L'idrogeno è costituito da molecole formate da due atomi tenuti insieme da un forte legame covalente. L'idrogeno molecolare è il più leggero dei gas: ad esempio, pesa ben 14 volte meno.
Preparazione dellidrogeno
Vi sono metodi facili ma costosi per preparare l'idrogeno e metodi difficili ma economici se praticati su vasta scala. I primi si usano in laboratorio e gli altri si sfruttano nell'industria.
In laboratorio si ottiene generalmente puro, facendo reagire lo zinco metallico con un acido forte, usando l'apparecchio di Kipp.
![]()
Si sceglie lo zinco perché costa poco ed ha un potenziale di riduzione inferiore a quello dell'idrogeno.
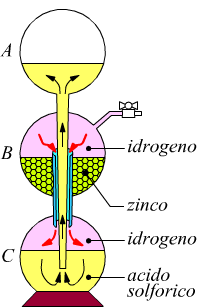
Nel disegno seguente è rappresentato l'apparecchio di Kipp, utile alla produzione di idrogeno in laboratorio. Nella boccia B vengono immessi dei pezzetti di zinco mentre dalla boccia A si lascia colare in C acido cloridrico o solforico, il quale, venendo a contatto con lo zinco della boccia B, produce idrogeno. La figura mostra ciò che avviene a rubinetto chiuso: l'idrogeno prodotto comprime l'acido nella boccia C (frecce rosse) facendolo risalire in A (frecce nere) e interrompendo così il contatto tra l'acido e lo zinco.
Industrialmente, l'idrogeno, si prepara facendo passare del vapore surriscaldato su carbone coke,
![]()
Poiché la reazione è endotermica (ΔH°=131,3kJ) (ΔG°=91,6 kJ) il suo rendimento aumenta a temperatura elevata; in pratica si opera a ∼1000°C. Si mantiene elevata la temperatura mediante la combustione di parte del carbone con dosate immissioni di aria.
La miscela CO+H2 contenente anche basse percentuali di CO2 è indicata anche come gas d'acqua; viene sottratta all'equilibrio, addizionata ancora di una opportuna quantità di vapor d'acqua e fatta passare su catalizzatori (a base di ferro e/o cobalto) a ∼400°C. Si ha, allora, la reazione detta reazione di conversione del gas d'acqua.
![]() (ΔH°=-41
kJ)
(ΔH°=-41
kJ)
La reazione globale tra C ed H2O è dunque:
![]() (ΔH°=90,2
kJ)
(ΔH°=90,2
kJ)
che rappresenta la reazione di preparazione dell'idrogeno mediante il processo del gas d'acqua detto anche processo di gassificazione del carbone.
L'idrogeno si può anche preparare tramite un processo denominato reforming del metano che si ottiene facendo reagire il metano (CH4) con l'acqua .
![]()
Questo processo, (ΔH°=204,6kJ e ΔG°=142,3 kJ) dagli anni settanta ha conquistato il primo posto per la preparazione industriale dell'idrogeno. Si tratta di una reazione endotermica ed il relativo equilibrio è fortemente spostato verso sinistra a bassa temperatura, mantenuta mediante combustione di calcolate quantità di metano ed in presenza di catalizzatori (Sali di nichel supportati su ossido di alluminio).
L'idrogeno, può anche essere ottenuto industrialmente per via elettrolitica, ma soltanto come sottoprodotto di elettrolisi effettuate per la produzione di altri prodotti; infatti la preparazione elettrolitica dell'idrogeno da soluzioni acquose, senza che all'anodo si ottenga qualche prodotto più pregiato dell'ossigeno, non è economicamente conveniente.
I composti dell'idrogeno
L'idrogeno nei suoi legami compare in tre stati di ossidazione: +1, 0 e -1. Con lo stato di ossidazione +1 lo troviamo nella maggior parte dei suoi composti, nei quali si trova combinato con un elemento più elettronegativo. A parte l'acqua, i composti più importanti che lo contengono sono il metano (CH4) e tutti gli altri idrocarburi, l'ammoniaca (NH3), gli aci- di inorganici e gli idrossidi. Con lo stato di ossidazione -1 lo si trova combinato con gli elementi meno elettronegativi con cui forma gli idruri (molto usati nelle sintesi organiche) tra cui i più importanti sono: l'idruro di sodio (NaH), l'idruro di litio e alluminio (LiAlH4). Con lo stato di ossidazione 0 lo si trova nella molecola biatomica H2.
Proprietà dell'idrogeno
L'idrogeno a temperatura ordinaria reagisce spontaneamente solo col fluoro:
![]()
Con l'ossigeno reagisce in maniera esplosiva, dando H2O, se la miscela viene innescata da una scintilla elettrica. Con il cloro reagisce ad alta temperatura o a seguito di irradiazione,
![]()
cioè la reazione viene innescata dalla luce ma poi prosegue spontaneamente.
Con l'azoto si combina ad alta temperatura, sotto pressione, ed in presenza di catalizzatori, dando luogo all'ammoniaca.
![]()
Uso dell'idrogeno
Come elemento, allo stato gassoso, lo si usava in passato per riempire dirigibili e palloni aerostatici ma a causa della sua alta infiammabilità è stato in seguito sostituito dall'elio.
Industrialmente la maggior parte dell'idrogeno oggi prodotto è impiegata per la sintesi diretta dell'ammoniaca, dell'acido cloridrico, del metanolo e per la trasformazione degli oli vegetali in margarina.
Puro, allo stato liquido, l'idrogeno generalmente viene utilizzato in miscela con l'ossigeno liquido come propellente per razzi vettori che mettono in orbita i satelliti artificiali.
Come deuterio è impiegato nella preparazione dell'acqua pesante (D2O), utilizzata come moderatore dei neutroni nei reattori nucleari, mentre come trizio trova sempre più largo impiego in esperimenti di radiochimica, di biologia e di medicina in quanto questo isotopo presenta una massa ben tre volte maggiore di quella del protio e, quindi, le differenze tra le proprietà fisiche e chimiche dei composti dell'idrogeno e dei composti marcati con trizio sono facilmente riscontrabili.
L'idrogeno si usa, comunemente, per produrre la fiamma ossidrica, adoperando
l'omonimo cannello ("cannello ossidrico ").
Per questi utilizzi viene commercializzato in bombole di acciaio, alla pressione
di 150 atm, contraddistinte da una fascia di colore rosso nella parte superiore.
 edutecnica
edutecnica